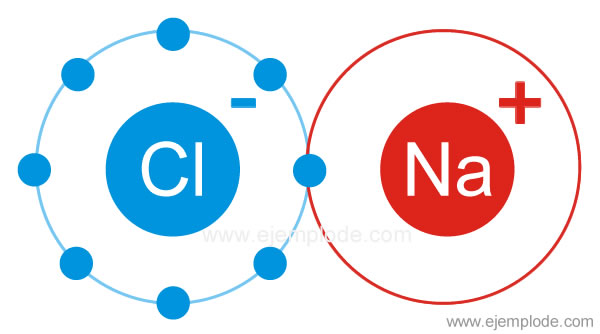
Ejemplos de enlaces iónicos
Los enlaces iónicos se producen cuando se encuentran átomos de elementos metálicos, con no metálicos. Esta unión se debe a la atracción electrostática que se produce cuando los átomos de un metal ceden electrones a los átomos de un no metal, creándose iones de diferente carga.
La atracción de los iones de diferente carga eléctrica es muy grande y hace que estos átomos queden fuertemente unidos.
Las sustancias creadas a partir de este tipo de enlace reciben el nombre de compuestos iónicos y a las fuerzas eléctricas que realizan esta unión se les denomina enlaces iónicos.
Características del enlace iónicos:
-Está formado por metal y no metal.
-No forma moléculas verdaderas, existe como un agregado de aniones (iones negativos) y cationes (iones positivos).
-Los metales ceden electrones formando cationes, los no metales aceptan electrones, a su vez, formando aniones.
Características de los compuestos formados por los enlaces iónicos:
-Son sólidos a temperatura ambiente, ninguno es líquido o gas.
-Son muy buenos conductores del calor y la electricidad.
-Tienen altos puntos de fusión y de ebullición.
-Son solubles en solventes polares, como el agua.
Por ejemplo, la sal común es formada cuando los átomos de gas cloro, se ponen en contacto con los átomos de metal sodio. Y se forma así el compuesto NaCl, es decir, la sal común. Reaccionan los átomos de sodio con los átomos de cloro, formándose iones de cargas opuestas y cada uno se rodea del máximo número de iones de signo contrario.
10 ejemplos de enlaces iónicos:
- Cloruro de Sodio (NaCl)
- Cloruro de Potasio (KCl)
- Ioduro de Potasio (KI)
- Óxido de Hierro (FeO)
- Cloruro de Plata (AgCl)
- Oxido de Calcio (CaO)
- Bromuro de Potasio (KBr)
- Óxido de Zinc (ZnO)
- Oxido de Berilio (BeO)
- Cloruro de Cobre (CuCl2)